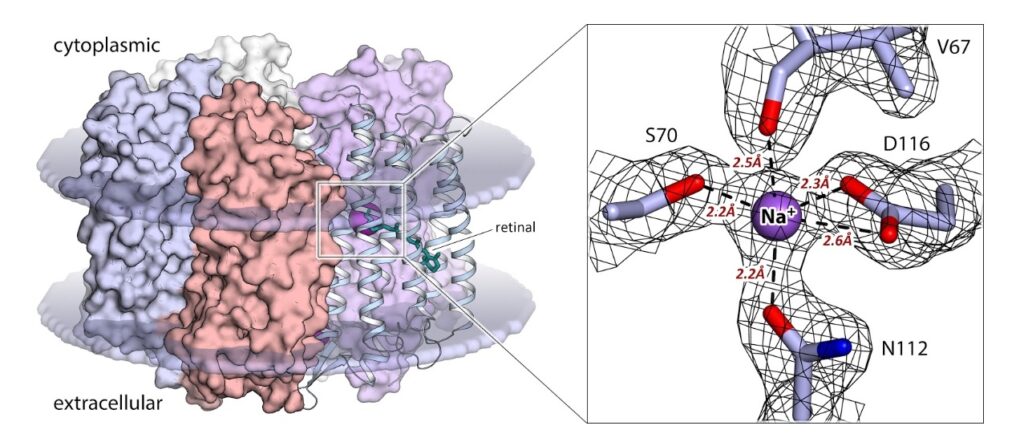
Пентамер родопсина KR2 в клеточной мембране (синие диски) в активном состоянии (слева). Сайт связывания натрия в активном центре белка (справа). Расстояния до координирующих натрий атомов кислорода указаны в Ангстремах. Карта электронной плотности показана черной сеткой. Ион натрия показан фиолетовой сферой. Источник: Кирилл Ковалев ©
Международная группа ученых впервые получила структуру светочувствительного белка-транспортера натрия KR2 в активном состоянии. Это позволило описать механизм переноса ионов натрия через клеточную мембрану под воздействием света. Работа ученых опубликована в одном из самых престижных научных журналов — Nature Communications.
KR2 принадлежит к огромному семейству микробных родопсинов — светочувствительных белков, находящихся в клеточной мембране архей, бактерий, вирусов и эукариот. Эти белки способны выполнять широкий спектр функций, но наиболее интересной является перенос различных ионов через мембрану под воздействием света. Именно такие ионные каналы и насосы являются инструментами оптогенетики — одной из самых актуальных биомедицинских дисциплин, позволяющей управлять активностью различных типов клеток организма при облучении их светом. Широкую известность оптогенетика обрела благодаря значительному вкладу в развитие методов минимально инвазивных исследований мозга, а также лечения таких нейродегенеративных заболеваний, как болезни Альцгеймера, Паркинсона, и прочие. Более того, сегодня оптогенетика позволяет восстанавливать потерянные слух, зрение и мышечную активность.
К сожалению, несмотря на описанные успехи, развитие оптогенетики усложняется ограниченным набором белков, которые могут быть использованы для активации и ингибирования клеток организма. К примеру, наиболее широко используемый инструмент оптогенетики — канальный родопсин 2 — способен одновременно транспортировать ионы натрия, калия и кальция, а также протоны. Его структура была впервые получена научными сотрудниками и выпускниками МФТИ и опубликована в ведущем научном издании Science. Низкая «избирательность» этого белка приводит к появлению нежелательных вторичных (побочных) эффектов при работе с клетками. Таким образом, оптимизация протоколов использования оптогенетических инструментов на сегодняшний день требует огромного количества средств и времени.
Поиск новых, более селективных белков для оптогенетики является приоритетным направлением в этой области исследований. Родопсин KR2, найденный в 2013 году, является уникальным оптогенетическим инструментом, так как позволяет при физиологических условиях избирательно переносить через клеточную мембрану исключительно ионы натрия. Понимание механизмов его работы очень важно для оптимизации функциональных характеристик этого белка, а также для создания на его основе новых оптогенетических инструментов.
Биофизики МФТИ в 2015 и 2019 годах опубликовали первые структуры KR2 в различных формах. В том числе они показали, что белок формирует пентамеры, находясь в мембране. Более того, образование таких комплексов необходимо для функционирования родопсина. Однако во всех описанных авторами моделях белок находился в неактивированном, то есть основном состоянии. Для понимания принципов транспорта ионов через мембрану была необходима также структура активного состояния белка, так как натрий переносится родопсином только после активации последнего светом. Именно такая кристаллическая структура высокого разрешения и была получена и описана учеными.
«Изначально мы использовали классический подход, активируя KR2 в заранее выращенных белковых кристаллах, освещая их лазером и фиксируя активное состояние путем быстрой заморозки кристалла при 100К, — рассказывает первый автор работы, аспирант МФТИ Кирилл Ковалев. — Нам повезло, ведь зачастую подобные манипуляции приводят к разрушению кристаллов. Для избежания этого нам пришлось аккуратно подбирать длину волны и мощность лазерного излучения, а также регулировать время засветки».
Такие эксперименты требуют большого количества белковых кристаллов высокого качества. Уникальное оборудование Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ позволило провести массивную кристаллизацию родопсина KR2.
Наиболее значимой находкой исследователей стала идентификация аминокислотных остатков белка, связывающих ион натрия внутри молекулы KR2. Именно они определяют селективность родопсина к определенному типу ионов. Кроме того, структура активного состояния высокого разрешения (2.1Å) позволила определить точную конфигурацию сайта связывания иона натрия в активном центре белка. Ученые впервые показали, что сайт связывания, образуемый KR2, идеально оптимизирован к ионам натрия в ходе эволюции родопсинов. Таким образом, именно полученная структура активного состояния должна использоваться для рационального дизайна оптогенетических инструментов нового поколения на основе KR2.
«Позже в ходе работы мы получили структуру KR2 в активном состоянии при комнатной температуре, — продолжает Кирилл Ковалев. — Для этого нам пришлось модернизировать известные протоколы сбора кристаллографических данных. Также мы воспользовались набирающими популярность методами серийной кристаллографии на источнике синхротронного излучения».
Структура активного состояния KR2, полученная при комнатной температуре, подтвердила верность модели белка, определенной ранее при низкой температуре. Это помогло ученым напрямую продемонстрировать, что криозаморозка не влияет на внутреннее устройство родопсина.
Полученные структуры позволили впервые описать механизм активного транспорта ионов натрия через клеточную мембрану под действием света. Так, исследователи показали, что перенос натрия родопсином наиболее вероятно осуществляется по гибридному механизму, включающему в себя принципы как эстафетного транспорта протонов, так и пассивной диффузии ионов через полярные полости в белке. Предложенный авторами механизм был подтвержден с помощью функциональных исследований мутантных форм KR2, а также компьютерного моделирования процесса высвобождения ионов натрия из белка.
«Транспорт ионов через мембранную стенку — фундаментальный биологический процесс. При этом перенос ионов натрия должен иметь принципиально иной механизм, чем таковой для протонов, — поясняет Валентин Горделий, директор исследований в Институте структурной биологии в Гренобле и научный координатор Центра исследований молекулярных механизмов старения и возрастных заболеваний в МФТИ. — Мы впервые увидели, как ион натрия связывается внутри молекулы родопсина, а также показали механизм выброса ионов в межклеточное пространство».
Авторы уверены, что результаты их работы не только раскрывают фундаментальные принципы, лежащие в основе ионного транспорта через клеточную мембрану, но и имеют практическую пользу для нужд оптогенетики. Ученые МФТИ продолжают разработку оптимизированных форм белка KR2 для расширения арсенала методов изучения головного мозга и лечения нейродегенеративных заболеваний.
В работе принимали участие ученые из Московского физико-технического института (МФТИ), Института структурной биологии Гренобльского университета и Европейского ускорительного комплекса в Гренобле (Франция), Юлихского исследовательского центра, Аахенского университета, Института Макса Планка, Европейской лаборатории молекулярной биологии (Германия), а также источника синхротронного излучения ALBA (Испания).
Работа была поддержана Министерством науки и высшего образования РФ и Российским фондом фундаментальных исследований.

