Исследователи обнаружили новый биомаркер в спинномозговой жидкости, который предсказывает когнитивное снижение при болезни Альцгеймера лучше прежних маркеров. Это соотношение двух белков, YWHAG и NPTX2, точнее предсказывающее как быстрый регресс одних пациентов, так и когнитивную стабильность других.
Болезнь Альцгеймера — опасное нейродегенеративное заболевание. При этом мы не знаем, почему возникает эта болезнь, не до конца понимаем её течение, да и с прогнозом много сложностей. На сегодняшний день главными виновниками болезни считаются два белка — бета-амилоид и тау-белок, аномальные формы и скопления которых (бляшки и клубки) в тканях мозга коррелируют с деградацией мышления и памяти.
Амилоид и тау одновременно и главные биомаркеры, по которым оценивают течение болезни. Но хотя корреляция между их количеством и тяжестью болезни есть, она объясняет только от 20 до 40% вариативности когнитивных нарушений, то есть разницы между тяжестью симптомов и темпом их развития у разных пациентов. Поэтому, ориентируясь на них, спрогнозировать утрату памяти для больных и их близких (болезнь Альцгеймера может передаваться по наследству, поэтому все родственники пациента автоматически оказываются в группе риска), затрудняет понимание болезни и вызывает у медиков и фармакологов ряд проблем. Низкая точность усложняет и поиск лекарства, и клинические испытания препаратов. Нынешние лекарства от БА нацелены именно на борьбу с двумя упомянутыми белками, и их эффективность лишь умеренная, порядка 20-30% у препаратов последних лет.
«Поиск протеомных биомаркеров очень интересное и, на мой взгляд, перспективное направление, — говорит Елена Петерсен, заведующая лабораторией молекулярно-биологических и нейробиологических проблем и биоскрининга ИББ МФТИ, — поскольку позволяет подойти к диагностике заболевания задолго до старта его клинического проявления. Это достаточно сложное дело, поскольку не всегда получается выявить точные связи, и можно говорить только о корреляции. Кроме того, помимо самого наличия заболевания, поиск биомаркеров к которому является основной целью, необходимо учитывать такие факторы, как пол, возраст, возможно этническую принадлежность, поскольку компенсаторные механизмы на различного рода повреждения у представителей разных этнических групп могут реализовываться по-разному».
Существуют крупные лонгитюдные исследования, например Исследование монахинь и ROSMAP (Religious Orders Study and Memory and Aging Project), которые показывают, что накопление амилоида и тау напрямую не коррелирует со снижением умственных способностей. Тут надо отметить, что «когнитивное снижение» (cognitive decline) — это ухудшение работы памяти, контроля внимания, речи и ряда других способностей, которое регистрируется при помощи стандартизированных тестов (например MMSE).
Есть пациенты, которые даже не смотря на наличие классических биомаркеров БА, сохраняют свои когнитивные способности и прекрасно справляются с соответствующими тестами до глубокой старости.
Именно сложность поиска точных связей делает исследование, опубликованное в журнале Nature Medicine, столь актуальным. Оно посвящено биомаркерам, которые позволили бы предсказывать когнитивное снижение у пациентов с БА, и вообще узнать что-то новое об устройстве этой болезни. Авторы провели анализ спинномозговой жидкости и плазмы крови у 3,4 тысяч испытуемых из разных демографических когорт. Они изучали протеом, то есть белковый состав ликвора и плазмы, и объединили данные с другими параметрами: результатами когнитивных тестов, уровнями бета-амилоидов и тау, возрастом, полом и генетическим статусом (наличие аллели APOE4 и мутации ADAD, которые коррелируют с риском болезни Альцгеймера).
Протеомный анализ показал, что больше всего коррелировали с когнитивной функцией белки, которые отвечают за функции синапсов. Особенно выделялись два из них: NPTX2 и YWHAG.
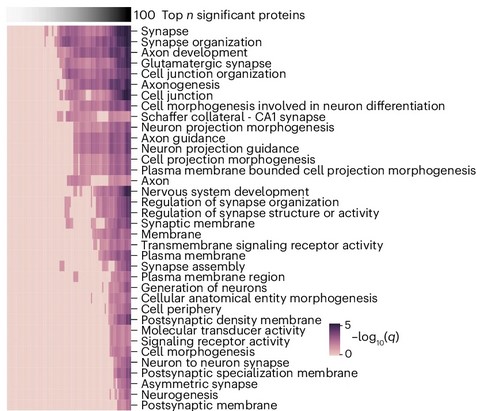
Сравнительное количество разных групп белков в ликворе. Как видно, синаптических белков больше всего.
Изображение: Oh, H.SH., Urey, D.Y., Karlsson, L. et al / Nature Medicine, 2025
NPTX2 — это белок из семейства нейрональных пентраксинов, синтезируемых в нейронах для поддержки синапсов в нормальном состоянии. NPTX2 образуется в ответ на возбуждение и регулирует активность синапсов, снижая активность особо возбуждённых нейронов. Без этого белка нейронные связи человека подвержены гипервозбудимости (как, например, при эпилепсии), которую микроглия (макрофаги ЦНС) подавляет, уничтожая синапсы. В результате количество связей между нейронами уменьшается, а это сказывается и на когнитивных функциях. Второй белок, YWHAG, изучен хуже. Известно, что мутации в его гене вызывают эпилепсию, и он участвует в агрегации тау-белка.
С возрастом содержание NPTX2 падает, а значит ухудшается регуляция возбуждения. Количество белка YWHAG, предположительно связанного с патологическими процессами, остаётся прежним, и вместе это приводит к снижению количества синапсов и, следовательно, когнитивному снижению.
Учёные прогнали данные через методы машинного обучения и те указали на новый биомаркер — соотношение YWHAG:NPTX2. Этот показатель не зависит от количества бета-амилоидов и тау-белков, и превосходит их по предсказательной силе на 27%. Кроме того, новый биомаркер оказался более «красноречивым»: если наличие патологии амилоидов и тау увеличивет риск деменции в 4 раза, то риск у 25% испытуемых с самым высоким отношением YWHAG:NPTX2 выше уже в 15 раз.
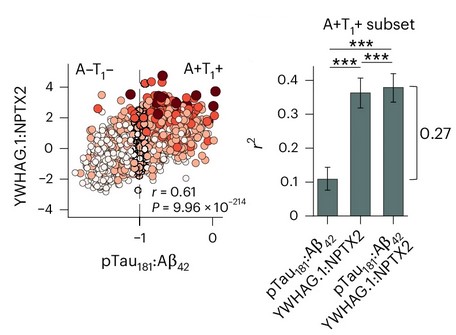
Сравнение точности нового биомаркера по сравнении с классическими (бета-амилоиды и тау-белки)
Изображение: Oh, H.SH., Urey, D.Y., Karlsson, L. et al / Nature Medicine, 2025
Сравнение точности нового биомаркера в сравнении со старым, по амилоидам и тау. Изображение: Oh, H.SH., Urey, D.Y., Karlsson, L. et al.
Исследование дало новый биомаркер и показало, что болезнь Альцгеймера, видимо, связана не столько с наличием аномальных белков, сколько с разрушением связей между нейронами.
«В данной работе исследователи определяли мультипротеиновую синаптическую сигнатуру снижения когнитивных функций, — поясняет Петерсен, — и таким образом могли анализировать не только количественное распределение белков, но и их соотношение. Полученные результаты, касающиеся соотношения белков синаптической щели YWHAG:NPTX2, позволяют их рассматривать как дополнительную прогностическую клиническую метрику при предсказании развития или старта первичных проявлений болезни Альцгеймера с большей чувствительностью чем до этого, что дает больше времени пациенту для коррекции своего состояния».
Правда, высокая точность нового биомаркера показана только для спинномозговой жидкости. В плазме учёные также обнаружили связь между белками YWHAG, NPTX2 и когнитивными нарушениями, но корреляция белков плазмы с биохимическими процессами в мозгу устроена сложнее, и по словам авторов статьи, для создания надёжных маркеров по анализам крови нужны дополнительные исследования.

